우리 세포 속에는 생명의 유통기한을 기록하는 타이머가 존재합니다. 바로 염색체 끝에 달린 '텔로미어(telomere)'입니다. 신발 끈 끝의 플라스틱 캡처럼 유전 정보를 보호하는 텔로미어는 세포가 분열할 때마다 조금씩 짧아지며, 이것이 한계에 다다르면 세포는 노화 상태에 접어듭니다.
과학자들은 이 노화 과정을 늦추거나 되돌릴 방법을 찾고 있지만, 연구에 적합한 동물 모델을 찾는 것은 큰 난관이었습니다. 기존 모델은 노화가 너무 느리거나, 반대로 너무 허약해 실험이 불가능한 경우가 많았죠. 최근 한 연구팀이 이 '골디락스' 문제에 대한 해답을 제시했습니다. 바로 노화는 빠르지만 유충 단계에서 약물 효과를 검증할 만큼은 생존하는, 아주 특별한 제브라피쉬 모델을 개발한 것입니다.
이 글에서는 2025년 Aging Cell에 실린 Hernández-Silva, D.외의 논문 " Development of a short telomere zebrafish model for accelerated aging research and antiaging drug screening"를 바탕으로 노화 관련된 최신 연구를 살펴봅니다.
완벽한 노화 모델을 찾아서: ST2 제브라피쉬의 탄생
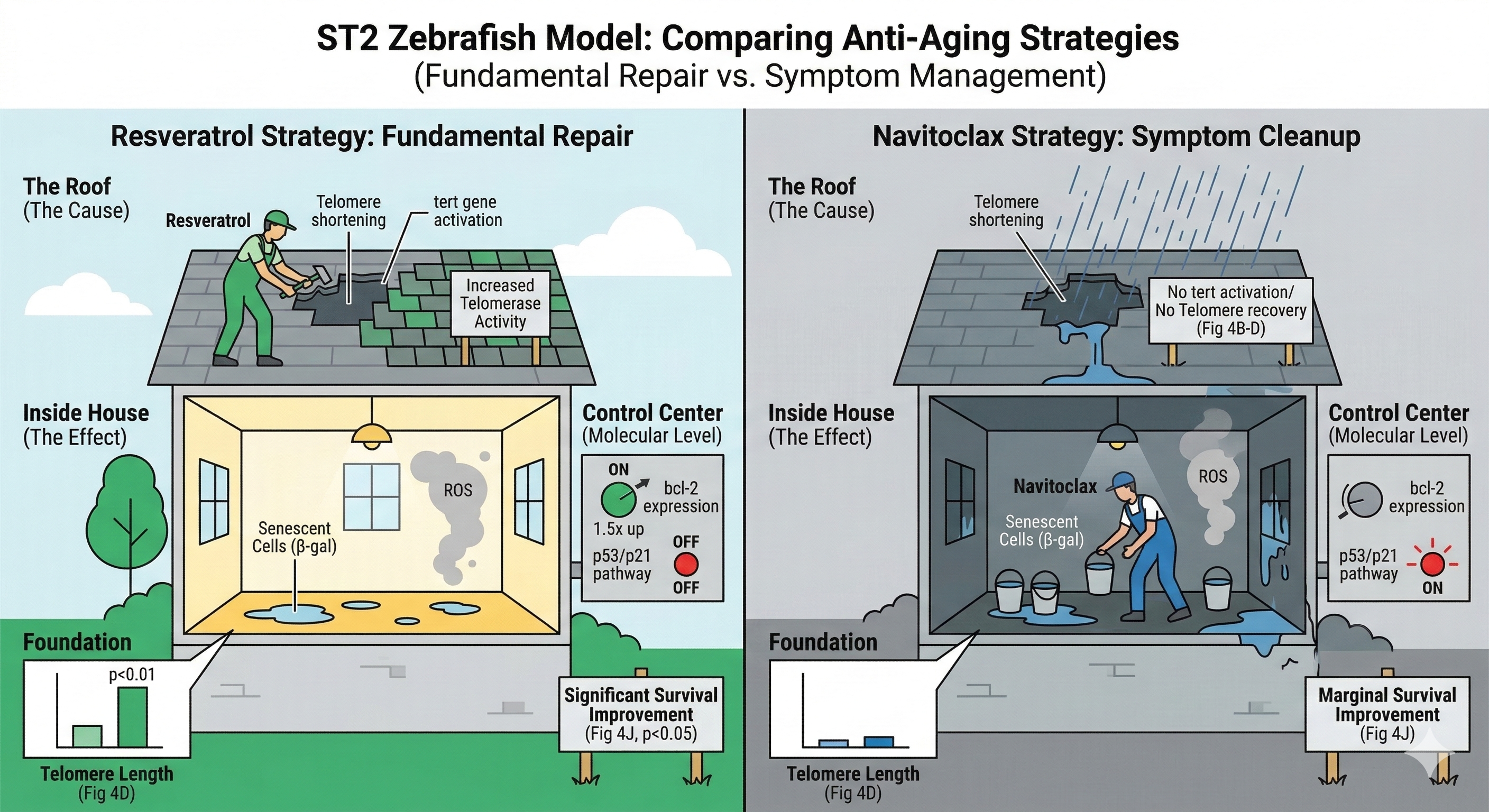
그림 1
연구팀은 이 ST2 노화 모델을 이용해 두 가지 항노화 전략을 시험했습니다. 첫 번째는 텔로미어 길이를 직접 복구하는 레스베라트롤(Resveratrol), 두 번째는 이미 생성된 노화세포를 제거하는 나비토클락스(Navitoclax)입니다. 그림 1은 두 전략의 효과가 극명하게 갈렸음을 보여줍니다.
레스베라트롤은 텔로미어 복구 효소 유전자인 `tert`의 발현을 약 2배 가까이 촉진했으며, 이는 실제 텔로머레이스 활성도와 텔로미어 함량의 유의미한 증가로 이어졌습니다. 이러한 근본적인 개선은 노화세포(β-gal), 활성산소(ROS), 세포사멸(AO) 지표의 현저한 감소라는 결과로 나타났습니다. 분자 수준에서는 `p53`과 `p21` 경로를 억제하고, 세포 생존을 돕는 `bcl-2` 유전자 발현을 1.5배 이상 높였습니다.
반면, 나비토클락스는 노화세포와 세포사멸을 줄이는 데는 효과적이었지만, 핵심 원인인 텔로머레이스 활성이나 텔로미어 길이를 회복시키지는 못했습니다. 최종적으로 장기 생존율 평가에서 레스베라트롤은 대조군 대비 생존율을 유의미하게 향상시킨 반면, 나비토클락스의 효과는 미미했습니다.
이는 텔로미어 단축이 노화의 핵심 원인일 경우, 증상을 완화하는 것보다 근본 원인을 해결하는 것이 더 효과적인 치료 전략임을 명확히 보여줍니다.
조기 노화의 '지문': 짧아진 텔로미어와 그 여파
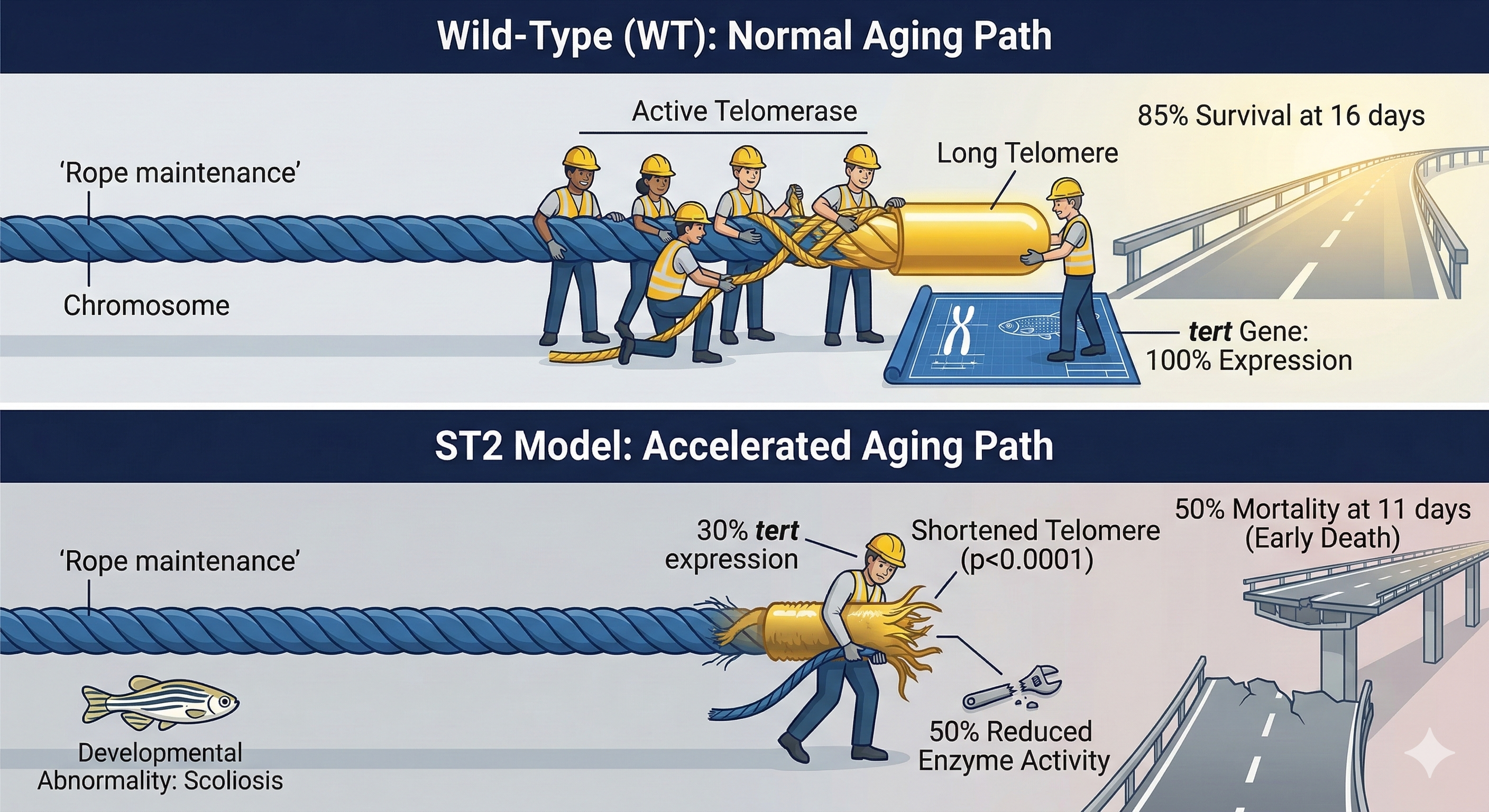
그림 2
그림 2는 ST2 모델의 특징을 명확히 보여줍니다. ST2 유충은 일부에서 척추가 휘는 등의 발달 이상을 보였고, 생존율 또한 급격히 감소했습니다. 정상(WT) 유충이 16일 후에도 85% 이상 생존한 반면, ST2 유충은 약 11일 만에 절반이 사망하는 조기 사망 현상을 나타냈습니다.
이러한 현상의 근본 원인은 텔로미어 유지 능력의 저하에 있었습니다. ST2 유충은 텔로머레이스 효소를 만드는 `tert` 유전자의 발현량이 정상 대비 약 30% 수준으로 급감했으며, 이로 인해 효소의 실제 활성도 역시 절반 수준으로 떨어졌습니다.
가장 결정적인 증거는 텔로미어 길이 자체였습니다. 세대를 거듭하며 텔로미어는 점진적으로 짧아졌는데, ST2 모델의 텔로미어 길이는 정상(WT)의 절반에도 미치지 못할 뿐만 아니라, 이전 세대인 ST1보다도 유의미하게 짧아져 있었습니다. 이는 ST2 모델의 조기 노화와 사망이 짧아진 텔로미어 때문임을 직접적으로 증명하는 결과입니다.
두 가지 항노화 전략의 시험대: 레스베라트롤 대 나비토클락스
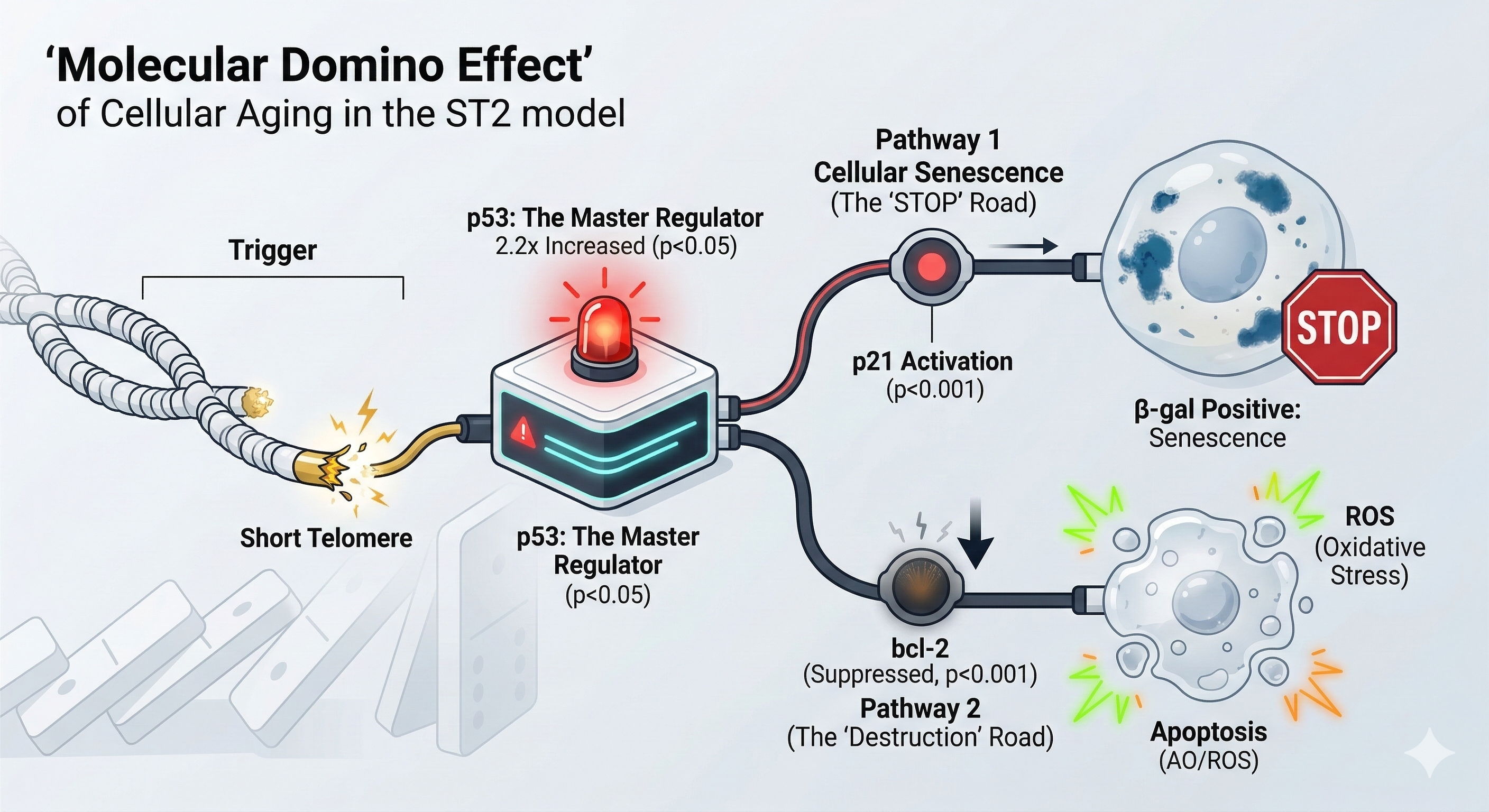
그림 3
짧아진 텔로미어는 세포 수준에서 어떤 연쇄 반응을 일으킬까요? 그림 3은 ST2 모델의 세포에서 나타나는 노화의 징후들을 종합적으로 보여줍니다.
먼저, 노화 세포의 지표인 β-gal 염색에서 ST2 유충은 정상(WT)보다 훨씬 넓고 진한 파란색 신호를 보이며, 이는 통계적으로도 유의미한 증가를 나타냈습니다. 이는 ST2 모델에서 세포 노화가 가속화되었음을 시사합니다. 세포 스트레스 수준 역시 높았습니다. 활성산소(ROS)를 탐지하는 염색과 세포 사멸(apoptosis)을 나타내는 AO 염색 모두에서 ST2 유충은 정상보다 현저히 강한 형광 신호를 보였습니다. 이는 세포들이 심각한 산화 스트레스에 시달리며 죽어가고 있음을 의미합니다.
이러한 현상의 분자적 원인은 실험 결과로 추정할 수 있습니다. DNA 손상 반응의 핵심 조절자인 `p53` 유전자와 그 하위 표적인 `p21`의 발현이 ST2에서 약 2.2배씩 크게 증가한 반면, 세포 사멸을 억제하는 `bcl-2` 유전자의 발현은 절반 수준으로 급감했습니다.
종합하면, 짧아진 텔로미어가 `p53` 경로를 활성화시켜 세포 노화와 사멸을 촉진하는 '도미노 효과'를 일으킨 것입니다.
결론

이번 연구는 단지 새로운 동물 모델을 개발한 것을 넘어, 노화 치료 전략에 대한 중요한 통찰을 제공합니다. ST2 제브라피쉬 모델은 텔로미어 단축이 생존을 결정하는 핵심 요인일 때, 단순히 노화 세포를 제거하는 것만으로는 충분하지 않다는 것을 명확히 보여주었습니다. 근본 원인인 '짧아진 텔로미어'를 직접 해결하는 레스베라트롤과 같은 접근법이 더 효과적이었던 것입니다.
물론 이는 제브라피쉬 유충 단계의 실험 결과이며 인간의 노화에 바로 적용할 수는 없습니다. 하지만 ST2 모델은 앞으로 텔로미어 생물학에 기반한 새로운 항노화 약물 후보물질을 빠르고 효율적으로 탐색하는 강력한 도구가 되어, 건강 수명 연장의 꿈에 한 걸음 더 다가가는 발판을 마련해 주었습니다.
정리 논문 : Hernández-Silva, D., López-Abellán, M. D., Martínez-Navarro, F. J., García-Castillo, J., Cayuela, M. L., & Alcaraz-Pérez, F. (2025). Development of a short telomere zebrafish model for accelerated aging research and antiaging drug screening. Aging Cell, 24, e70007. https://doi.org/10.1111/acel.70007

